2006-11-17 Ostatnia modyfikacja.
Zadanie
Zadanie.  Model Bohra.
Model Bohra.
W modelu atomu wodoru Bohra orbity, n = 1,2,3,... są oznaczone literami K, L, M,... . Dla elektronów na każdej z orbit K, L, M, oblicz:
a. promieniowanie orbit,
b. częstość obiegu,
c. prędkości liniowe,
d. momenty pędu,
e. całkowitą energię układu.
Rozwiązanie
Rozwiązanie
a. Pytanie jest nieprecyzyjnie sformułowany. Postulat Bohra mówi o tym, że elektrony poruszające się po orbitach nie promieniują energii (inaczej musiałyby spadać na jądro). Fotony są wyświecane wtedy, gdy następuje przejście elektronu z orbity wyższej na niższą. Można, więc wykorzystać wzór Rydberga do wyznaczenia długości fal wypromieniowanych przy przejściach:
![]()
![]()
![]()
b. Należy wyprowadzić wzór ogólny, pozwalający obliczyć promień dowolnej orbity Bohrowskiego wodoru. Należy to zrobić w oparciu o postulat mówiący o skwantowaniu momentu pędu elektronu na orbicie.
![]()
gdzie L jest momentem pędu na orbicie n.
Dla przypomnienia moment pędu jest iloczynem wektorowym promienia
wodzącego i pędu ![]() .
.
W przypadku toru będącego okręgiem wartość momentu pędu wyraża się jako
![]() .
.
Nie będę przeprowadzał całego wywodu dotyczącego wzoru na częstość obiegu (można go znaleźć w podręcznikach do szkoły średniej). Ograniczę się do podania wzoru.
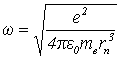
gdzie
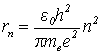
Po podstawieniu wielkości liczbowych otrzymamy
![]()
![]()
![]()
c.
Obliczenie prędkości liniowych polega jedynie na wymnożeniu
częstości ![]() przez promień
przez promień
![]()
![]()
![]()
![]()
d. Podstawiamy wartości do wzoru
![]()
![]()
![]()
![]()
e. Całkowita energia układu.
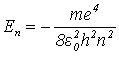
![]()
![]()
![]()
Odpowiedź
Dyskusja
Zadania z przedmiotu
Zadania