 Izoprocesy gazu doskonałego
Izoprocesy gazu doskonałego
Wśród
procesów termodynamicznych ważnością
i prostotą opisu i wyróżniają się izoprocesy
gazu doskonałego, czyli procesy, w trakcie
których jeden z parametrów gazu doskonałego
pozostaje stały.Zaliczamy do
nich proces izotermiczny, izobaryczny,
izochoryczny i – jeśli był
przeprowadzony kwazistatycznie –
proces adiabatyczny.Linki
prowadzą do bardziej wyczerpujących
opisów; w tym miejscu podajemy jedynie
skrótowe zestawienie.
|
proces |
definicja |
prawo |
równanie
stanu |
I zasada
termodynamiki |
uwagi |
|
izotermiczny |
T = const. |
Boyle’a-Mariotte’a |
pV = const. |
ΔU=0
|ΔQ|=|ΔW|
ΔW=nRTln(V2/V1)
|
rurka
Meldego |
|
izobaryczny |
p
= const. |
Gay-Lussaca |
V/T
= const. |
ΔW =pΔV=nRΔT
ΔQ=nCPΔT=mcPΔT
ΔU=nCV ΔT |
|
|
izochoryczny |
V
= const. |
Charlesa |
p/T
= const. |
ΔW=0
ΔU=ΔQ=nCVΔT
ΔU=nCV ΔT
|
termometr
gazowy |
|
adiabatyczny |
ΔQ = 0 |
Poissona |
pVk = const. |
ΔU=ΔW
ΔW=nCV ΔT=CVΔ(pV)/R |
|
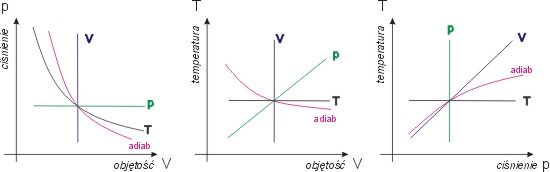
Na
rysunkach poniżej wykresy izoprocesów
w różnych zmiennych.
Izochorę oznaczono kolorem niebieskim,
izobarę - zielonym, izotermę - czarnym,
a adiabatę - czerwonym.
|